ENERGI DALAM
Perubahan energi dalam dapat diketahui dengan mengukur kalor (q) dan kerja (w), yang akan timbul bila suatu sistem bereaksi. Oleh karena itu, perubahan energi dalam dirumuskan dengan persamaan E = q + w.
Jika sistem menyerap kalor, maka q bernilai positif. Jika sistem mengeluarkan kalor, maka q bernilai negatif.
Jika sistem melakukan kerja, maka w pada rumus tersebut bernilai positif. Jika sistem dikenai kerja oleh lingungan, maka w bernilai negatif.
Jadi bila suatu sistem menyerap kalor dari lingkungan sebesar 10 kJ, dan sistem tersebut juga melakukan kerja sebesar 6 kJ, maka perubahan energi dalam-nya akan sebesar 16 kJ.
Perubahan energi dalam bernilai 0 jika jumlah kalor yang masuk sama besar dengan jumlah kerja yang dilakukan, dan jika kalor yang dikeluarkan sama besar dengan kerja yang dikenakan pada sistem. Artinya, tidak ada perubahan energi dalam yang terjadi pada sistem
ENTROPI
Entropi adalah salah satu besaran termodinamika yang mengukur energi dalam sistem per satuan temperatur yang tak dapat digunakan untuk melakukan usaha. Mungkin manifestasi yang paling umum dari entropi adalah (mengikuti hukum termodinamika), entropi dari sebuah sistem tertutup selalu naik dan pada kondisi transfer panas, energi panas berpindah dari komponen yang bersuhu lebih tinggi ke komponen yang bersuhu lebih rendah. Pada suatu sistem yang panasnya terisolasi, entropi hanya berjalan satu arah (bukan proses reversibel/bolak-balik). Entropi suatu sistem perlu diukur untuk menentukan bahwa energi tidak dapat dipakai untuk melakukan usahapada proses-proses termodinamika. Proses-proses ini hanya bisa dilakukan oleh energi yang sudah diubah bentuknya, dan ketika energi diubah menjadi kerja/usaha, maka secara teoritis mempunyai efisiensi maksimum tertentu. Selama kerja/usaha tersebut, entropi akan terkumpul pada sistem, yang lalu terdisipasi dalam bentuk panas buangan.
ENTALPI
Entalpi dari suatu sistem homogen didefinisikan sebagai:
di mana:
- H = entalpi sistem (joule)
- U = energi dalam (joule)
- P = tekanan dari sistem (Pa)
- V = volume sistem (
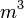 )
)
Entalpi adalah properti ekstensif yang berarti untuk sistem homogen, besarnya berbanding lurus dengan ukuran sistem. Terkadang digunakan juga entalpi spesifik h =H/mdengan m adalah massa sistem, atau entalpi molar Hm = H/n, dengan n adalah jumlah mol (h dan Hm adalah properti intensif. Untuk sistem tak homogen, entalpi adalah jumlahan entalpi dari beberapa subsistem
dengan k merujuk pada beberapa subsistem. Pada kasus untuk nilai p, T, dan komposisi yang berbeda-beda maka jumlah menjadi integral:
dengan ρ adalah densitas.
Entalpi H(S,p) dari suatu sistem homogen dapat diturunkan sebagai fungsi karakteristik S dan tekanan p sebagai berikut: kita mulai dari hukum pertama termodinamika untuk sistem tertutup
Disini, δQ adalah sejumlah kecil panas yang ditambahkan dalam sistem dan δW adalah sejumlah kerja yang dilakukan sistem. Untuk sistem homohen hanya proses reversibel yang dapat berlangsung sehingga hukum kedua termodinamika menyatakan δQ = TdS dengan T adalah temperatur absolut sistem. Jika hanya kerja PV yang ada, δW = pdV. Sehingga
Menambahkan d(pV) di kedua sisi sehingga menjadi
atau
Maka
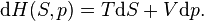
- Contoh :Tinjau air panas dalam termos. Anda tidak dapat mengatakan bahwa air dalam termos mengandung banyak kalor sebab panas yang terkandung dalam air termos bukan kalor, tetapi energi internal. Jika terjadi perpindahan panas dari air dalam termos ke lingkungan sekitarnya atau dicampur dengan air dingin maka akan terbentuk kalor.Besarnya kalor ini diukur berdasarkan perbedaan suhu dan dihitung menggunakan persamaan berikut.Q = m c ΔTKeterangan :Q = kalorm = massa zatc = kalor jenis zatΔT = selisih suhu


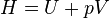
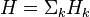
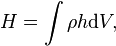


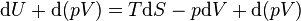
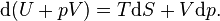
esgvSDvsdv cheer cheer
ReplyDeleteLick my blurb x-)
ReplyDelete